DELInsight|聚焦固相DNA编码化合物库构建,探索高纯度多肽库构建新路
DEL Insight | 聚焦固相DNA编码化合物库构建,探索高纯度多肽库构建新路
随着传统的DNA编码化合物库(DEL)化学领域日趋成熟,对于库的质量的期望也变得越来越高。除了传统上专注于纯化方案和反应产率的优化之外,越来越多的研究团队开始探索采用固相合成策略来提高多肽库的纯度。本文中,我们将探讨从最近的三篇关于固相DEL衍生物的文章中获得的一些见解。
Chen Shiyu课题组提出了一种用于DNA编码多肽库(PDELs)的固相纯化策略,通过设计一种带有末端叠氮基团的修饰Fmoc(mFmoc)保护基团来实现1。这种设计使得在每一步偶联反应后,可以通过无铜点击化学将所需的多肽中间体特异性地与炔基功能化固定在可控孔玻璃(CPG)珠上(图1)。经过严格洗涤去除未反应的砌块和截短的副产物后,通过标准Fmoc去保护步骤释放纯产物。这种“捕获-释放”循环成功获得了五轮构建后的PDEL,其纯度超过95%,有效地突破了传统的四轮合成障碍。(Solid DEL-1)

图1:使用mFmoc保护的氨基酸,通过迭代循环生成纯化的DNA编码肽库。在固定化和纯化后,分离得到所需的DNA编码肽(Solid DEL-1)。
J rg Scheuermann团队开发了另一种在磁珠上进行的双连接固相合成策略,以实现DELs的“自纯化”释放(图2)2。这一固相平台不仅实现了高纯度五轮目标多肽化合物的合成,还显著扩展了反应兼容范围——可兼容无水条件,从而使传统水相DEL合成中无法进行的反应(如SnAP环化反应和酸介导的Boc去保护)成为可能。(Solid DEL-2)
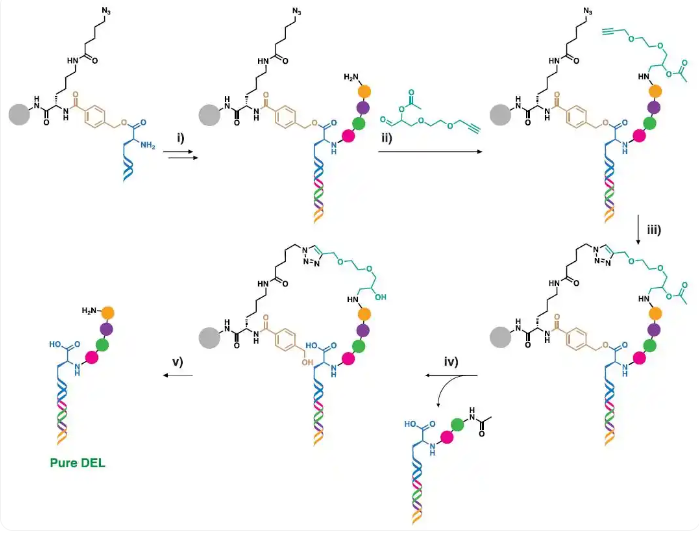
图2:用于“自纯化”释放DEL的合成策略(Solid DEL-2)。
Brian M. Paegel开创了一种替代的固相DEL合成策略,该策略集成了“一珠一化合物”(OBOC)方法3。通过这种策略,每个库成员分子均在固相微珠上构建,并通过光裂解连接子与DNA标签相连。这种设计便于所需多肽化合物的物理分离以及通过光触发释放相应的分子,从而支持更广泛的筛选模式,包括基于活性的测定和细胞表型筛选。不过,这种方法需要对离散物理珠上的化合物进行单独筛选,因此本质上会受到库的规模限制,只能达到104到106个。(图3)(Solid DEL-3)
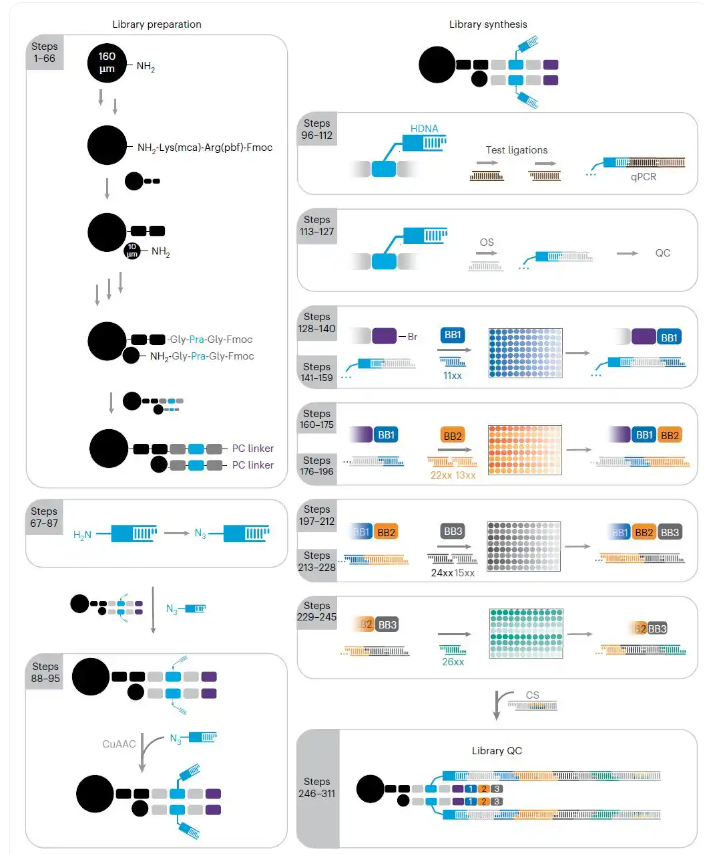
图3:用于“一珠一化合物”的DEL合成策略(Solid DEL-3)。
总体而言,这三种固相DEL设计范式为未来的多肽DEL库构建带来了新启示:我们可以战略性地利用新兴技术,从根本上提高多肽DEL库的质量。顺应这一发展趋势,成都先导也在探索引入新颖的固相方法来提升自身多肽库的质量。我们预计,在不久的将来,这些创新将成功付诸实践,为下一代DEL合成开辟新的方向。
引用文献:
1. He Q, Wang Y, Tang X, et al. Enhanced screening via a pure DNA-encoded peptide library enabled by an Fmoc modification. Proc Natl Acad Sci U S A. 2026;123(8):e2524999123. doi:10.1073/pnas.2524999123
2. Keller M, Petrov D, Gloger A, et al. Highly pure DNA-encoded chemical libraries by dual-linker solid-phase synthesis. Science. 2024;384(6701):1259-1265. doi:10.1126/science.adn3412
3. Dixit A, Paegel BM. Solid-phase DNA-encoded library synthesis: a master builder's instructions. Nat Protoc. 2026;21(2):542-581. doi:10.1038/s41596-025-01190-4

